Các nhà khoa học đang tiến gần tới khả năng áp dụng chỉnh sửa bộ gen cho một mục tiêu đầy thách thức: bộ não con người. Nỗ lực này nhằm giúp điều trị các căn bệnh nguy hiểm.
Trong hai năm qua, hàng loạt tiến bộ công nghệ và kết quả đầy hứa hẹn trên chuột đã đặt nền tảng cho việc điều trị các rối loạn não nghiêm trọng bằng các kỹ thuật bắt nguồn từ chỉnh sửa gen CRISPR–Cas9. Các nhà nghiên cứu hy vọng các thử nghiệm trên người sẽ chỉ còn cách vài năm nữa.
“Dữ liệu chưa bao giờ trông tốt như bây giờ,” Monica Coenraads, người sáng lập kiêm giám đốc điều hành của Rett Syndrome Research Trust tại Trumbull, Connecticut, nói. “Điều này ngày càng ít mang tính khoa học viễn tưởng và gần với thực tế hơn.”
Thách thức đáng gờm
Các nhà nghiên cứu đã phát triển liệu pháp chỉnh sửa gen để điều trị các bệnh về máu, gan và mắt. Tháng 5 vừa qua, các nhà khoa học báo cáo thành công ngoạn mục khi sử dụng liệu pháp chỉnh sửa gen cá nhân hóa để điều trị cho một bé trai tên KJ mắc bệnh gan hiểm nghèo.
Nhưng bộ não đặt ra những thách thức đặc biệt. Các thành phần phân tử cần thiết để điều trị cho KJ được đưa vào các hạt mỡ tự nhiên tích tụ trong gan. Các nhà nghiên cứu đang tìm kiếm những hạt tương tự có thể nhắm mục tiêu chọn lọc vào não, vốn được bao quanh bởi một hàng rào phòng thủ ngăn nhiều chất xâm nhập.
Mặc dù câu chuyện của KJ rất thú vị, nhưng cũng gây thất vọng cho những gia đình có người thân mắc bệnh thần kinh, Coenraads – người chuyên về hội chứng Rett, một rối loạn hiếm gặp ảnh hưởng đến phát triển não – cho biết. Bà nói: “Câu hỏi tôi thường nghe từ các gia đình là: ‘Việc điều trị cho bé ấy nhanh thế. Tại sao chúng tôi lại mất lâu đến vậy?’”
Số lượng gia đình quan tâm đang tăng lên khi bác sĩ và phụ huynh ngày càng sử dụng giải trình tự bộ gen để tìm nguyên nhân các rối loạn não trước đây từng là bí ẩn, Cathleen Lutz, nhà di truyền học tại The Jackson Laboratory ở Bar Harbor, Maine, nói. “Chẳng hạn, mọi người đang bắt đầu nhận ra rằng các cơn co giật của con họ liên quan đến các đột biến gen cụ thể,” bà nói.
Tiến triển trên chuột
Các nghiên cứu trên chuột gợi ý rằng công nghệ chỉnh sửa gen, có thể viết lại những đoạn nhỏ trong bộ gen của tế bào, đã sẵn sàng để sửa một số đột biến này. Tháng 7 vừa qua, các nhà nghiên cứu báo cáo họ đã sửa các đột biến gây ra một chứng bệnh liệt nửa người luân phiên ở trẻ em (AHC). Bệnh này thường xuất hiện trước khi trẻ 18 tháng tuổi, gây co giật, khó khăn học tập và các cơn liệt một phần. “Đây là một căn bệnh khủng khiếp,” David Liu, nhà sinh hóa học tại Broad Institute của MIT và Harvard ở Cambridge, Massachusetts, nói.
Liu và đồng nghiệp sử dụng một nhánh chỉnh sửa gen của CRISPR trên chuột mang đột biến gây AHC. Kỹ thuật này sửa đột biến ở khoảng một nửa vỏ não, khu vực điều khiển học tập và trí nhớ. Chuột cũng thể hiện cải thiện nhiều chỉ số: cơn co giật giảm mức độ nghiêm trọng, nhận thức và kiểm soát vận động tốt hơn, tuổi thọ kéo dài. “Kết quả trên chuột thật ấn tượng,” Liu nói. “Chúng tôi thực sự ngạc nhiên.”
Phòng thí nghiệm của Liu cũng đang nghiên cứu trên chuột để sửa các đột biến gây hai rối loạn thần kinh khác: bệnh Huntington và bệnh ataxia Friedreich ở người. Bệnh Huntington là một bệnh di truyền thần kinh tiến triển, do đột biến gen HTT, gây rối loạn vận động và suy giảm nhận thức, và thường xuất hiện ở người trưởng thành từ 30–50 tuổi. Trong khi đó, Ataxia Friedreich là một bệnh di truyền thần kinh hiếm gặp liên quan đến đột biến gen FXN, khiến bệnh nhân đi lại khó khăn, yếu cơ, run, nói khó, và đôi khi gây ra bệnh tim cơ.
Tại Trường Y khoa Đại học Giao thông Thượng Hải, nhà thần kinh học Zilong Qiu và các đồng nghiệp đã sử dụng chỉnh sửa nền để sửa đột biến trong gen MEF2C.
Ở chuột đực, các đột biến này làm thay đổi hành vi xã hội của chúng. Việc sửa đột biến MEF2C bằng chỉnh sửa nền (base editing) – phiên bản cực kỳ chính xác của CRISPR có thể chỉnh sửa từng ký tự DNA – giúp khôi phục hành vi xã hội bình thường và cải thiện kết nối giữa các tế bào thần kinh. Qiu và Liu cũng đang độc lập phát triển liệu pháp chỉnh sửa gen cho hội chứng Rett, thường do đột biến gen MECP2 gây ra.
Việc đơn giản thêm một bản sao MECP2 bình thường theo liệu pháp gen thông thường có thể khiến tế bào sản xuất quá nhiều protein tương ứng và có thể độc hại. Nhưng chỉnh sửa gen chỉ sửa bản sao tự nhiên của gen và ít khả năng gây sản xuất quá mức MECP2, Qiu nói.
Khó khăn về tài chính
Từ kết quả trên chuột tới thử nghiệm lâm sàng trên người là một chặng đường dài. Qiu hy vọng nhóm của ông sẽ sẵn sàng trong khoảng năm năm tới để thử liệu pháp chỉnh sửa nền trên người mắc hội chứng Rett. Nhóm của Liu hy vọng trong vài năm tới có thể hoàn thành các thí nghiệm còn lại để tiến hành nghiên cứu trên người mắc AHC.
Do các hạt mỡ như trong liệu pháp của KJ chưa phải lựa chọn khả thi, cả hai nhóm dự đoán các thử nghiệm lâm sàng sẽ sử dụng một loại virus gọi là adeno-associated virus 9 (AAV9) để đưa các thành phần chỉnh sửa gen vào não. Virus này có thể xâm nhập tế bào não và phần nào vượt qua hàng rào máu–não.
Tuy nhiên, AAV9 cũng tiềm ẩn rủi ro, vì liều cao có thể gây phản ứng miễn dịch nguy hiểm. Các nhà nghiên cứu đang chạy đua để phát triển các virus cải tiến sử dụng liều thấp hơn. Tổ chức của Coenraads cũng đang tài trợ nghiên cứu phương pháp không dùng virus để đưa phân tử vào tế bào não.
Cuối cùng, rào cản lớn nhất có thể không phải về công nghệ. Ở Mỹ, ngành công nghệ sinh học đang trải qua giai đoạn khủng hoảng tài chính kéo dài. Một số nhà đầu tư đã rút khỏi các liệu pháp gen và phương pháp chỉnh sửa gen, vốn tốn kém và khó sản xuất.

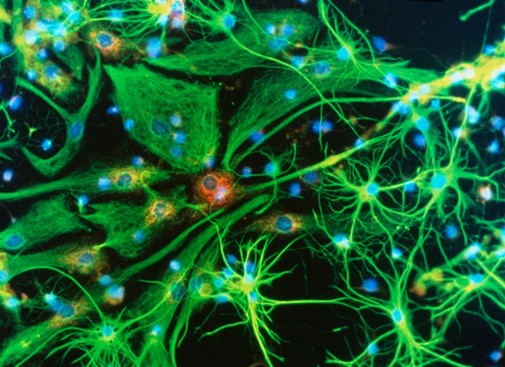
Tế bào não (tô màu nhân tạo) có thể bị nhiễm virus mang bộ công cụ để sửa các đột biến gây bệnh. Ảnh: Science Photo Library